优瑞科生物科技公司是一家开发创新 T 细胞疗法治疗实体肿瘤的临床分期生物科技公司,而希望之城则是美国最大的癌症研究和治疗组织之一,近日,两家机构携手宣布,希望之城已首次使用一种试验性 T 细胞疗法—— ECT204,对患有 GPC3 阳性晚期肝细胞癌(HCC)的患者完成给药。这标志着 GPC3 靶向 ARTEMIS® T 细胞首次用于人类 HCC 治疗,而 GPC3 阳性正是肝癌中最常见的类型之一。
磷脂酰肌醇蛋白聚糖 3(GPC3)存在于 70% 以上的 HCC 细胞中,因此对于 HCC 疗法来说,这是一个非常具有潜力的靶点。在其它的实体瘤如卵巢癌和肺癌中,科研人员也发现了 GPC3 蛋白。在评估 ECT204 的 ARYA-3 试验研究中,患者的 T 细胞经收集后被改造成表达优瑞科公司专有的、靶向 GPC3 的 ARTEMIS 细胞受体,然后注回至患者体内以靶向和杀死表达 GPC3 的癌细胞。今年 1 月,美国食品和药物管理局(FDA)授予 ECT204 为“唯一指定药品”(“孤儿药资格”)以治疗 HCC。关于这项 I/II 期研究的其他信息可以在ClinicalTrials.gov网站上查阅 NCT 标识符: NCT04864054。
优瑞科创始人兼首席执行官 Cheng Liu 博士表示:“首次给患者使用 ECT204,是我们致力于将 T 细胞治疗扩大到实体肿瘤的重要一步。在临床前研究中,ARTEMIS T 细胞已经证明了其优越的肿瘤浸润性和良好的安全性。我们期待在临床环境中对其进行进一步开发,以充分释放 T 细胞治疗实体肿瘤的潜力。”
“希望之城致力于寻找创新疗法来治疗具有挑战性的实体肿瘤。这些癌症目前没有有效的治疗药物。使用 T 细胞免疫疗法靶向 GPC3 将是治疗晚期肝癌的一种极具前景的方法。” 希望之城神经内分泌肿瘤项目的联合主任、ARYA3 试验首席研究员Daneng Li 医学博士表示。
肝癌是全球第四大癌症死亡原因,2020 年,大约有 83 万人死于肝癌。预计 2022 年美国将出现约 4.1 万例新增肝癌病例和近 3.1 万例肝癌死亡病例。根据美国癌症协会的统计,自 1980 年以来,肝癌确诊病例增加了两倍多。晚期 HCC 患者预后差,治疗选择有限。
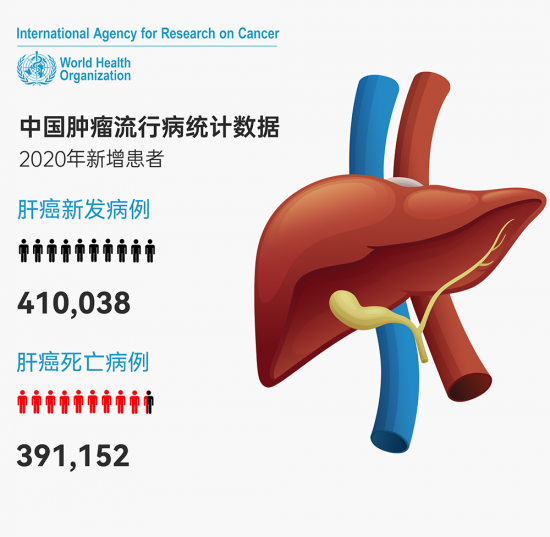
就中国而言,据世界卫生组织(WHO)国际癌症研究机构(IARC)GLOBOCAN 2020 中国报告,估计 2020 年有 410,038 例新发肝癌病例,并将导致约 391,152 例死亡。
“肝癌患者的治疗选择非常有限,迫切需要更多具有新颖作用机制的创新疗法,为这一具有挑战性的诊断带来希望。我非常期待使用这种实验疗法去治疗更多的患者以及看到相关的研究数据以了解 ECT204 的潜力。” Li 博士表示。

希望之城以为今日患者交付未来治愈方法为使命。自 1913 年成立以来,目前已经成为美国最大的癌症研究和治疗组织之一,同时也是针对糖尿病和其他威胁生命的疾病领先研究中心之一。作为一家由美国国家癌症研究所指定的独立综合性癌症中心,希望之城为患者带来了一套涵盖癌症护理、研究和开发、学术和培训以及创新计划在内的独特整合模式。由希望之城开发的相关研究和技术已经成为许多突破性癌症药物以及人类合成胰岛素和单克隆抗体的基础。作为骨髓移植和免疫治疗(CAR-T 细胞治疗)领域的领导者,希望之城的个体化治疗方案有助于促进全世界的癌症护理。
为了让最新发现和尖端护理惠及更多的患者、家庭及社区,希望之城正在扩张其全国系统,包括位于洛杉矶的主院区、南加州临床护理中心网络、位于加州橙郡的新癌症中心以及美国癌症治疗中心。此外,希望之城的附属机构还包括转化基因组学研究所和 AccessHopeTM。